(记者天津眼工作室 朱虹)2019年10月25日,天津大学生命科学学院青年教师刘斯与合作者在发现人源钾氯共转运蛋白KCC1的机理方面取得重要突破,她以第一作者身份在世界顶级学术期刊《科学》(《Science》)上发表研究论文,首次解析出人源钾氯共转运体蛋白KCC1的2.9埃冷冻电镜高分辨结构(1埃=10-10米),揭示了钾离子和氯离子在细胞膜蛋白上的结合位点,提出了钾-氯共转运机理,为癫痫等相关疾病治疗和药物设计提供了新的视角。
人体细胞内的钾、钠、氯等离子浓度处于相对平衡的状态,一旦失衡将会导致一系列疾病,如高血压、抑郁、癫痫等。在细胞膜上,有一类被称为阳离子-氯离子共转运蛋白的蛋白质,负责调控细胞内外的离子浓度。其对于维持细胞内外渗透压平衡,保障生物细胞活性至关重要。钾氯共转运体蛋白KCC1就是其中一种,“它们就像附着在细胞膜上的一个个门户,能够自主调节进出细胞的离子数量,维持细胞内外的稳态平衡。”刘斯说。
长期以来,由于缺乏精确的结构信息,人们对这类膜蛋白的工作机理认识非常有限。刘斯与课题组成员经过长期深入研究,依托单颗粒冷冻电镜技术,结合离子转运实验、分子动力学模拟、结构比较等方法成功解析出3个人源KCC1的原子分辨率结构,发现KCC1是以二聚体的形式存在,阐释了该转运蛋白以1:1的比例同时同向转运钾离子和氯离子的机理,提出了KCC1共转运钾离子和氯离子的模型。
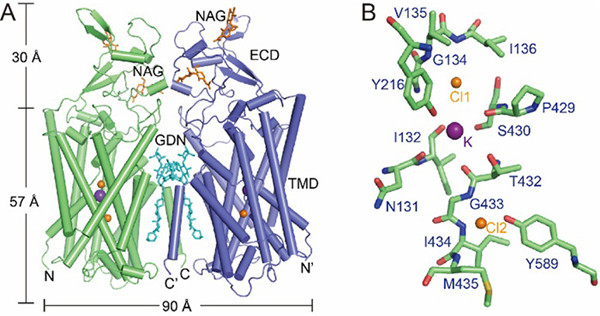
图1.人源KCC1的结构。(A)KCC1的二聚体结构;(B)KCC1的钾离子与氯离子结合位点。
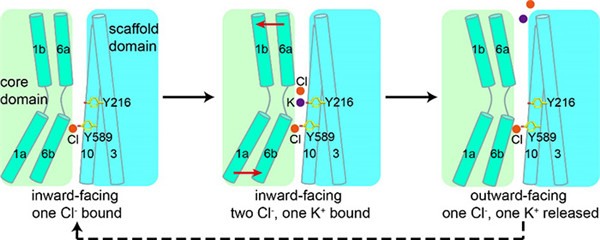
图2. KCC1共转运钾离子和氯离子的模型。第二个氯离子首先结合在第二位点,然后钾离子和第一个氯离子结合;KCC1的构象由内向态向外向态转变,钾离子和第一个氯离子释放至细胞外。
KCC1具有重要的生理功能,是临床上治疗癫痫等疾病的药物靶点。该研究成功解析出KCC1的蛋白结构,将有助于基于蛋白结构开展的药物研发,从而为临床上治疗相关疾病提供精准的数据支持。据了解,全球有近6000万的癫痫病患者,基于结构生物学研发以阳离子-氯离子共转运蛋白为靶点的癫痫病治疗药物,具有巨大的现实意义和应用价值。
人民日报中央厨房:https://www.hubpd.com/c/2019-10-25/929379.shtml
(编辑 焦德芳 王芷璇)

