近日,天津大学医学部生命科学学院王汉杰、刘夺团队与龙岩学院生命科学学院黄翠琴、尹会方团队合作,在《Chemical Engineering Journal》发文“Programmable therapeutic protein delivery in intestine via amplifier-optimized optogenetic bacteria and LED-equipped electronic capsule”[1]。该研究设计构建了一种含有“光控放大器”基因回路的工程菌,可在智能手机远程控制的“简易版”电子胶囊发光照射下,在肠道中分泌与递送治疗蛋白。该研究是王汉杰、刘夺团队继最近在Nature Microbiology发表“工程菌-电子胶囊双向交流”的“菌-机接口”研究[2]后,同步优化工程菌与胶囊设计以提升治疗干预效率的一个研究案例。
1.研究背景
合成生物学策略已开发出多种“治疗细菌”底盘作为活体药物,治疗干预胃肠道疾病、代谢病、癌症、神经系统疾病等疾病。光遗传学策略凭借高时空分辨率成为提高活体药物可控性的优选方法,仍面临挑战:(1)蛋白表达瓶颈:传统光控回路激活目标蛋白表达效率受限,单位时间内蛋白产量不足;(2)组织穿透障碍:可见光在组织(尤其胃肠道)中穿透性差。现有解决方案局限:近红外光遗传系统或植入式装置无法覆盖肠道深处,在大动物应用中受限。核心需求:开发光学生物电子接口系统,整合基因回路设计与非侵入式光传递技术。
2.研究内容
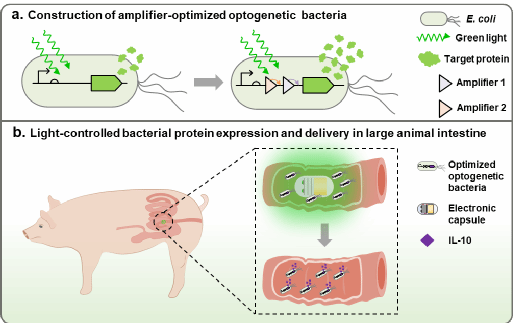
(1)工程菌“光控放大器”基因回路设计
本研究在大肠杆菌Nissle 1917 中构建了基于绿光(535 nm)诱导的基因转录系统。研究人员通过引入双层转录放大器模块,显著提升了目标蛋白表达效率。装载“光控放大器”的工程菌中报告蛋白GFP的表达激活时间可从40分钟缩短至10分钟,约1.5小时光照后最终表达激活倍数为22.7倍(原对照是7.6倍)。生物相容性海藻酸钠微珠封装的工程菌在光照20-40分钟内可实现100%响应蛋白表达。
针对治疗性蛋白分泌,经过测试,装载“光控放大器”的工程菌分泌报告蛋白GFP的起始时间可由3小时提前至1.5小时,Western-Blot验证最早10-20分钟即可产生分泌量差异。装载“光控放大器”的工程菌表达抑炎因子IL-10的分泌量可在1小时内达41.5倍提升(原对照是7.0倍)。小鼠吞服同等剂量工程菌时,仅装载“光控放大器”的工程菌可在光照30分钟内检测到肠道原位表达的荧光素酶信号,1小时达到峰值,显著强于其他分组。
研究人员进一步利用DSS诱导的小鼠结肠炎模型测试工程菌功能。通过小鼠每日口服IL-10分泌型光控菌+1小时绿光照射,光控放大模块工程菌分组的疗效显著。疾病活动指数(DAI)降幅61.9%(未加放大器工程菌组35.0%),便血评分降低58.3%(未加放大器工程菌组33.3%),体重恢复至初始97.1%(其他组≤92.7%),组织学分析显示:治疗组隐窝结构重建、粘膜完整性恢复,比其他分组的干预效果都要好,证实光控工程菌的抗炎治疗潜力。
(2)“简易版”发光电子胶囊功能检验
本研究设计并组装了集成电池、电压转换器、蓝牙模块及LED阵列的双层电路板电子胶囊。全功能模式(蓝牙连接+4 LED开启)下功耗稳定于2.5 mA,单次供电可持续工作>24小时,满足大型动物胃肠道应用需求。胶囊光照强度随距离呈指数衰减特性,确保对邻近光控菌的精准局部激活,避免非靶向组织照射。该电子胶囊的通信性能可保证80毫米范围内保持稳定蓝牙连接,可穿透猪组织实时激活LED。
研究人员进一步在离体模型(猪肠组织)内,利用电子胶囊发光成功诱导邻近工程菌中报告GFP的表达。通过生物安全性考察,胶囊发光90分钟内,其表面温度<32℃,无热毒性风险,且胶囊发光功率明显小于市售胶囊肠镜镜头光照功率。最终,研究人员测试了向猪结肠共递送胶囊与放大器优化工程菌,光照1小时使肠道IL-10分泌显著提升,为大型动物肠道局部光控触发治疗性蛋白递送提供了一条可行路径。
结论:针对光控蛋白表达瓶颈与光信号组织穿透障碍的难题,本研究的主要创新点在于:提出协同优化工程菌与电子胶囊的方案,一方面设计构建“光控放大器”基因回路显著增强工程菌目标蛋白产量,缩短光控蛋白饱和分泌的响应时间;另一方面设计构建“简易版”电子胶囊实现体内非侵入式光信号递送,该胶囊尺寸明显小于团队之前构建的“双向交流高配版”胶囊尺寸,且可进一步精简,有利于推向治疗应用。
本论文是团队在“菌-机接口”方向上进一步系统性优化的研究示例。伦敦帝国理工学院的David Carreño教授和David T. Riglar教授在Nature Microbiology的News&Views评论[3]指出:工程菌-电子胶囊体系仍存在可改进空间,包括:(1)工程菌方面:以更稳定方式取代多拷贝质粒,降低使用量(如通过定植方式),特定基因失活以避免宿主损伤风险;(2)电子胶囊方面:优化能耗,压缩胶囊尺寸。本论文一方面通过工程菌回路设计使其可在更短时间内(1小时)达到饱和治疗物释放,降低工程菌使用量,更加精细化控制其工作窗口;另一方面也改进了胶囊尺寸,“简易版”胶囊的整体尺寸为15 mm × 10.5 mm。根据美国食品药品监督管理局(FDA)指南建议胶囊的最大尺寸为标准00号(长度约24 mm),本论文构建的胶囊尺寸已满足可吞服要求。
3.联合团队协作
论文通讯作者是天津大学医学部生命科学学院王汉杰教授、刘夺副研究员,以及龙岩学院生命科学学院黄翠琴教授、尹会方副教授,第一作者是天津大学医学部生命科学学院研究生冯志杰与薛慧敏。本工作是天津大学对口支援龙岩学院开展联合研究的成果,体现了两校生命科学学院的深度协作。天津大学负责光控工程菌的构建、小鼠模型实验、电子胶囊装配,龙岩学院负责将工程菌与电子胶囊用于猪模型的实验。两个院校协作开发的技术可助力于经济动物疾病防治,对于畜牧业发展具有重要价值。双方在农业领域的持续深度合作将为闽西革命老区相关产业发展提供技术支撑。研究获得国家重点研发计划“合成生物学”专项、国家自然科学基金以及天津市自然科学基金支持等项目支持。
相关链接:
[1] Programmable therapeutic protein delivery in intestine via amplifier-optimized optogenetic bacteria and LED-equipped electronic capsule. Chemical Engineering Journal, https://doi.org/10.1038/s41564-025-02057-w
[2] Ingestible optoelectronic capsules enable bidirectional communication with engineered microbes for controllable therapeutic interventions. Nature Microbiology, https://doi.org/10.1038/s41564-025-02057-w
[3] Remote control designer probiotics. Nature Microbiology, News&Views, https://www.nature.com/articles/s41564-025-02072-x
